
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Последнее изменение 2025-01-22 17:08.
В энтальпия образования для элемент в своем стихийном состоянии всегда будет 0 потому что для образования природного соединения не требуется энергии. Когда вещество сформированный из наиболее устойчивой формы своего элементы , изменение в энтальпия происходит.
Точно так же можно спросить, какие вещества имеют нулевую энтальпию образования?
Все элементы в своих стандартных состояниях (газообразный кислород, твердое тело углерод в виде графит и т. д.) имеют стандартную энтальпию образования, равную нулю, поскольку в их образовании нет никаких изменений.
Впоследствии возникает вопрос, какова энтальпия образования воды? Выбранная энтальпия образования ATcT на основе версии 1.118 термохимической сети
| Название вида | Формула | ΔжH ° (298,15 К) |
|---|---|---|
| Воды | H2O (кр., Экв. Давление) | -292.740 |
Соответственно, почему стандартная энтальпия образования алмаза не равна нулю, хотя он является элементом?
В стандартная энтальпия образования для элемент в его стандарт состояние НУЛЬ !!!! Итак, ΔH ° f для C (s, графит) равно нуль , но ΔH ° f для C (s, алмаз ) составляет 2 кДж / моль. Это потому, что графит стандарт состояние углерода, не алмаз.
Что это значит, когда Delta h равна нулю?
Они могут измерять только изменения энтальпии. Когда энтальпия положительна и дельта H больше, чем нуль , это средства что система поглощает тепло. Это называется эндотермической реакцией. Когда энтальпия отрицательна и дельта H меньше чем нуль , это средства что система выделяет тепло. Это называется экзотермической реакцией.
Рекомендуемые:
Почему наведенная ЭДС равна нулю при максимальном магнитном потоке?

Когда катушка находится в вертикальном положении, магнитный поток не изменяется (т. Е. ЭДС = 0), потому что катушка не «пересекает» силовые линии. Индуцированная ЭДС равна нулю, когда катушки перпендикулярны силовым линиям, и максимальной, когда они параллельны. Помните, что наведенная ЭДС - это скорость изменения магнитной индукционной связи
Почему ЭДС равна нулю, когда катушка проходит точно через центр магнита?
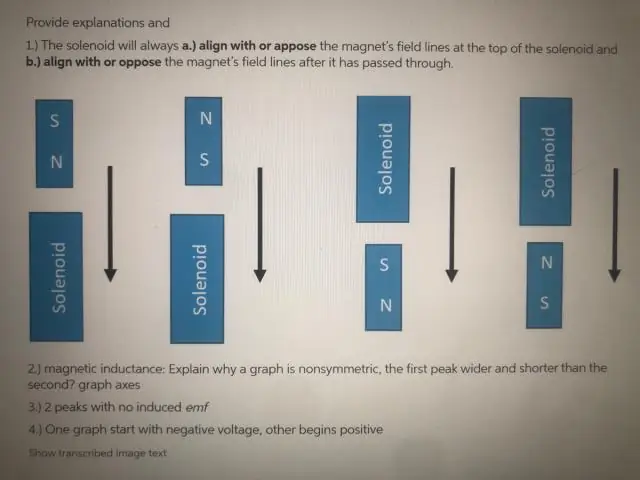
ЭДС равна нулю только на мгновение, когда магнит проходит точно через центр катушки. Это связано с тем, что влияние полюса N на одном конце магнита на этот конец катушки в точности компенсируется воздействием полюса S магнита на другой конец катушки
Какова стандартная энтальпия образования диоксида серы?

Для проверки оно должно быть (&минус; 296,81 ± 0,20) кДж / моль. Вам следует чаще использовать NIST. На самом деле я получил & минус 310,17 кДж / моль. Сначала вы должны найти Δ H∘f для SO3 (g)
Какова энтальпия образования Сао?

Таблица теплоты образования Соединение Δ Hf (кДж / моль) CaCO3 -1207,0 CaO (s) -635,5 Ca (OH) 2 (s) -986,6 CaSO4 (s) -1432,7
В каком процессе проделанная работа равна нулю?

Изохорный процесс (постоянный объем) Изохорический процесс - это процесс, в котором объем поддерживается постоянным, что означает, что работа, выполняемая системой, будет равна нулю. Изохорный процесс также известен как изометрический процесс или изоволюметрический процесс
