
- Автор Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Последнее изменение 2025-01-22 17:09.
Эти взаимодействия становятся возможными благодаря сворачиванию белковой цепи, чтобы сблизить удаленные аминокислоты. 2. Третичная структура стабилизируется дисульфидными связями, ионными взаимодействиями, водородные связи , металлические связи и гидрофобные взаимодействия.
Итак, какие взаимодействия стабилизируют третичную структуру белка?
Основная сила, стабилизирующая третичную структуру, - это гидрофобное взаимодействие между неполярными боковыми цепями в ядре белка. Дополнительные стабилизирующие силы включают электростатические взаимодействия между ионными группами с противоположным зарядом, водородные связи между полярными группами и дисульфид облигации.
Можно также спросить, какая из этих аминокислот участвует в ковалентном связывании, которое стабилизирует третичную структуру многих белков? Как и в случае дисульфидных мостиков, эти водородные связи может объединить две части цепочки, которые находятся на некотором расстоянии друг от друга с точки зрения последовательности. Солевые мостики, ионные взаимодействия между положительно и отрицательно заряженными участками боковых цепей аминокислот также помогают стабилизировать третичную структуру белка.
Учитывая это, как аминокислоты влияют на третичную структуру белка?
Когда-то неполярный аминокислоты сформировали неполярное ядро белок , слабые силы Ван-дер-Ваальса стабилизируют белок . Кроме того, водородные связи и ионные взаимодействия между полярными, заряженными аминокислоты внести свой вклад в третичная структура.
Как сохраняется третичная структура белка?
Объяснение: Третичная структура стабилизируется множественными взаимодействиями, в частности, функциональными группами боковых цепей, которые включают водородные связи , солевые мостики, ковалентные дисульфидные связи , и гидрофобные взаимодействия.
Рекомендуемые:
Кто открыл структуру ДНК-викторины?
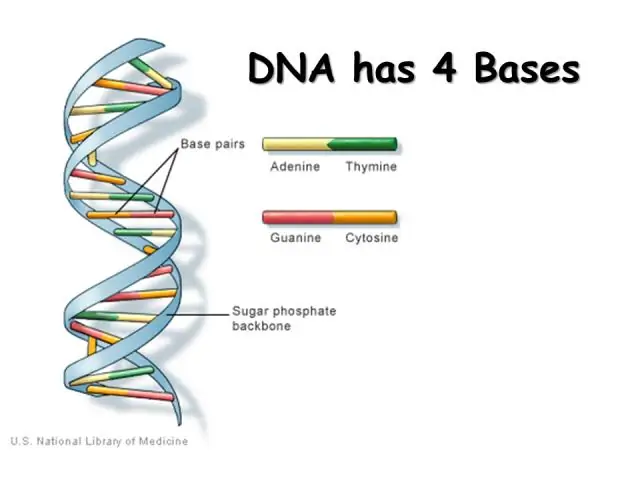
Ученые приписывают (опубликовано в 1953 году в журнале "Nature") открытие структуры ДНК. Хотя открытие принадлежало Уотсону и Крику, они не узнали бы о структуре, если бы не видели исследования Розалинды Франклин и Мориса Уилкинса
Какой тип связывания стабилизирует третичную структуру белка?

Третичная структура белка относится к общему трехмерному расположению его полипептидной цепи в пространстве. Обычно он стабилизируется внешнеполярным гидрофильным водородом и взаимодействиями ионных связей, а также внутренними гидрофобными взаимодействиями между боковыми цепями неполярных аминокислот (рис. 4-7)
Какая аминокислота C?

Коды аминокислот Ala A Аланин Cys C Цистеин Gln Q Глютамин Glu E Глутаминовая кислота Gly G Глицин
Какая сила наиболее влияет на определение третичной структуры белка?

Третичная структура белка - это трехмерная форма белка. Дисульфидные связи, водородные связи, ионные связи и гидрофобные взаимодействия влияют на форму, которую принимает белок
Какая аминокислота Агу?

Тройки оснований аминокислотной ДНК Кодоны M-РНК серин AGA, AGG, AGT, AGC TCA, TCG UCU, UCC, UCA, UCG AGU, AGC stop ATT, ATC, ACT UAA, UAG, UGA треонин TGA, TGG, TGT, TGC ACU , ACC, ACA, ACG триптофан ACC UGG
